
Статью подготовили специалисты образовательного сервиса Zaochnik.
Основные положения МКТ
Содержание:
Молекулярно-кинетическая теория – это учение о строении и свойствах вещества, основанное на представлении о существовании атомов и молекул, как наименьших частиц химических веществ.
Основные положения молекулярно кинетической теории строения вещества
Основные положения молекулярно-кинетической теории молекулы:
- Все вещества могут быть в жидком, твердом и газообразном состоянии. Они образуются из частиц, которые состоят из атомов. Элементарные молекулы могут иметь сложное строение, то есть иметь в своем составе несколько атомов. Молекулы и атомы – электрически нейтральные частицы, которые в определенных условиях приобретают дополнительный электрический заряд и переходят в положительные или отрицательные ионы.
- Атомы и молекулы движутся непрерывно.
- Частицы с электрической природой силы взаимодействуют друг с другом.
Основные положения мкт и их примеры были перечислены выше. Между частицами имеется малое гравитационное воздействие.

Рисунок Траектория Броуновской частицы.
Броуновское движение молекул и атомов подтверждает существование основных положений молекулярно кинетической теории и опытно обосновывает его. Данное тепловое движение частиц происходит с взвешенными в жидкости или газе молекулами.
Опытное обоснование основных положений молекулярно кинетической теории
В году Р. Броун открыл это движение, которое было обусловлено беспорядочными ударами и перемещениями молекул. Так как процесс происходил хаотично, то удары не могли уравновесить друг друга. Отсюда вывод, что скорость броуновской частицы не может быть постоянной, она постоянно меняется, а движение направления изображается в виде зигзага, показанное на рисунке
О броуновском движении говорил еще А. Эйнштейн в году. Его теория нашла подтверждение в опытах Ж. Перрена гг.
Следствие из теории Эйнштейна: квадрат смещения броуновской частицы относительно начального положения, усредненное по многим броуновским частицам, пропорционален времени наблюдения .
Выражение объясняет диффузионный закон. По теории имеем, что монотонно возрастает с увеличением температуры. Беспорядочное движение проглядывается при наличии диффузии.
Диффузия – это определение явления проникновения двух или нескольких соприкасающихся веществ друг в друга.
Данный процесс происходит быстро в неоднородном газе. Благодаря примерам диффузии с разными плотностями можно получить однородную смесь. При нахождении в одном сосуде кислорода и водорода с перегородкой то при ее удалении газы начинают смешиваться, образую опасную смесь. Процесс возможен при нахождении вверху водорода, а внизу кислорода.
Процессы взаимопроникновения также протекают в жидкостях, но намного медленней. Если растворить твердое тело, сахар, в воде, то получим однородный раствор, который является наглядным примером диффузионных процессов в жидкостях. При реальных условиях смешивание в жидкостях и в газах замаскировано быстрыми процессами перемешивания, к примеру, при возникновении конвекционных потоков.
Диффузия твердых тел отличается своей замедленной скоростью. Если поверхность взаимодействия металлов очистить, то можно увидеть, что с течением большого периода времени в каждом из них появятся атомы другого металла.
Диффузия и броуновское движение считаются родственными явлениями.
При взаимопроникновении частиц обоих веществ движение беспорядочно, то есть, наблюдается хаотичное тепловое перемещение молекул.
Броуновское движение
Силы, действующие между двумя молекулами, зависят от расстояния между ними. Молекулы имеют в своем составе положительные и отрицательные заряды. При больших расстояниях преобладают силы межмолекулярного притяжения, при небольших – силы отталкивания.
Рисунок показывает зависимость результирующей силы и потенциальной энергии взаимодействия между молекулами от расстояния между их центрами. На расстоянии сила взаимодействия обращается в ноль. Данное расстояние условно принимается в качестве диаметра молекулы. При потенциальная энергия взаимодействия минимальная.
Чтобы отдалить две молекулы с расстоянием , следует сообщить , называемую энергией связи или глубиной потенциальной ямы.
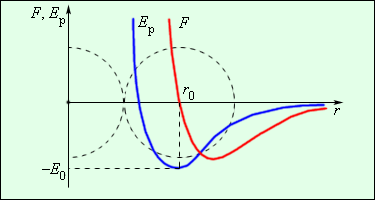
Рисунок Сила взаимодействия и потенциальная энергия взаимодействия двух молекул. – сила отталкивания, – сила притяжения.
Так как молекулы имеют малые размеры, то простые одноатомные могут быть не более . Сложные могут достигать размеров в сотни раз больше.
Беспорядочное хаотичное движение молекул называют тепловым движением.
При возрастании температуры увеличивается кинетическая энергия теплового движения. При пониженных температурах средняя кинетическая энергия, в большинстве случаев, оказывается меньше значения глубины потенциальной ямы . Данный случай показывает, что молекулы перетекают в жидкое или твердое вещество со средним расстоянием между ними . Если температура повышается, то средняя кинетическая энергия молекулы превышает , тогда они разлетаются и образуют газообразное вещество.
В твердых телах молекулы двигаются беспорядочно около фиксированных центров, то есть, положений равновесий. В пространстве может быть распределены нерегулярным образом (у аморфных тел) или с образованием упорядоченных объемных структур (кристаллических тел).
Агрегатные состояния веществ
Свобода теплового движения молекул просматривается в жидкостях, так как у них нет привязки к центрам, что позволяет производить перемещения по всему объему. Этим объясняется ее текучесть.
Если молекулы располагаются близко, то могут образовывать упорядоченные структуры с несколькими молекулами. Данное явление получило название ближнего порядка. Дальний порядок характерен для кристаллических тел.
Расстояние в газах между молекулами намного больше, поэтому действующие силы малы, а их движения идут вдоль прямой, ожидая очередного соударения. Значение является средним расстоянием между молекулами воздуха в нормальных условиях. Так как взаимодействие сил слабое, газы расширяются и могут заполнять любой объем сосуда. Когда их взаимодействие стремится к нулю, то говорят о представлении идеального газа.
Кинетическая модель идеального газа
В мкт количество вещества считается пропорциональным числу частиц.
Моль – это количество вещества, содержащее столько частиц (молекул), сколько содержится атомов в углерода . Молекула углерода состоит из одного атома. Отсюда следует, что моль вещества имеет одно и то же количество молекул. Данное число называется постоянной Авогадро .
Формула определения количества вещества записывается отношением числа частиц на постоянную Авогадро .
Массой одного моля вещества называют молярную массу . Она фиксируется в виде формулы .
Выражение молярной массы производится в килограммах на моль .
Если вещество имеет в составе один атом, тогда имеет место говорить об атомной массе частицы. Единица атома – это массы изотопа углерода , называется атомной единицей массы и записывается как (а. е. м.): .
Данная величина совпадает с массой протона и нейтрона.
Отношение массы атома или молекулы данного вещества к массы атома углерода называют относительной массой.
Навигация по статьям
