
Статью подготовили специалисты образовательного сервиса Zaochnik.
Опыт Резерфорда. Ядерная модель атома
Содержание:
Первая попытка создания модели атома была предпринята Дж. Томпсоном. Он полагал, что атом – это электронейтральная система формы шара с радиусом . На рисунке показано, как одинаково распределяется положительный заряд атома, причем отрицательные электроны располагаются внутри него. Чтобы получить объяснение линейчатых спектров атомов, Томпсон тщетно пытался определить расположение электронов в атоме, для расчета частоты их колебаний в положении равновесия. Спустя время Э. Резерфорд доказал, что заданная Томсоном модель была неверна.
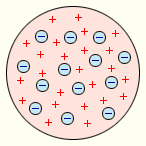
Рисунок Модель Дж. Томпсона.
Электроны в атоме. Опыты Резерфорда и Томпсона
Внутренняя структура атомов была исследована Э. Резарфордом, Э. Марсденом, Х. Гейгером еще в годах. Было применено зондирование атома -частицами, возникающими во время радиоактивного распада радия и других элементов. Их масса в раз больше массы электрона, а положительный заряд равняется удвоенному элементарному заряду.
В опытах Резерфорда были использованы -частицы, имеющие кинетическую энергию .
Альфа-частицы – это ионизированные атомы гелия.
Когда было изучено явление радиоактивности, этими частицами Резерфорд уже «бомбардировал» атомы тяжелых металлов. Входящие в них электроны не могут заменить траектории -частиц, так как имеют малый вес. Рассеяние может быть вызвано тяжелой положительно заряженной частью атома. На рисунке подробно описан опыт Резерфорда.
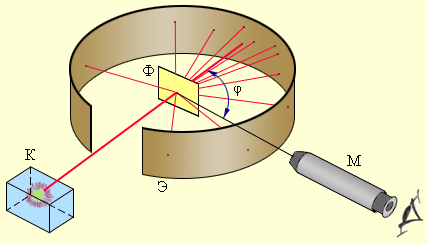
Рисунок Схема опыта Резерфорда по рассеянию -частиц. – свинцовый контейнер с радиоактивным веществом, – экран, покрытый сернистым цинком, – золотая фольга, – микроскоп.
Радиоактивный источник, заключенный в свинцовый контейнер, располагается таким образом, что
-частицы направляются от него к тонкой металлической фольге. Рассеянные частицы попадают на экран со слоем кристаллов сульфида цинка, светящиеся от их ударов. Сцинтилляции (вспышки) можно наблюдать при помощи микроскопа. Угол к первоначальному направлению пучка не имеет ограничений для данного опыта.
После испытаний было выявлено, что -частицы, проходящие через тонкий слой металла, не испытывали отклонений. Наблюдались их отклонения и на углы, превышающие градусов и близкие к .
Модели атомов Томпсона и Резерфорда
Результат Резерфорда противоречил модели Томпсона, так как положительный заряд не был распределен по всему объему атома. Согласно модели Томпсона, заряд не имеет возможности создавать сильное электрическое поле, которое впоследствии отбросит -частицы. Такое поле однородно заряженного шара максимально на его поверхности и убывает до нуля к центру.
При уменьшении радиуса шара с положительным зарядом атома максимальная сила отталкивания, действующая на -частицы, по закону Кулона увеличилась бы в раз.
Если размеры -частиц достаточно большие, тогда рассеивание может достичь угла в градусов.
Резерфорд пришел к выводу, что пустота атома связана с наличием положительного заряда, сосредоточенного в малом объеме. Данная часть была названа атомным ядром.
Далее возникла ядерная модель атома, показанная на рисунке
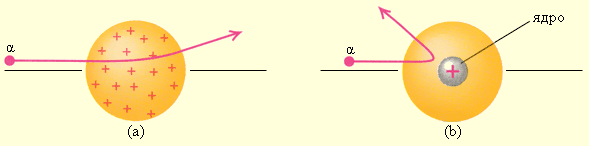
Рисунок Рассеяние -частицы в атоме Томсона и в атоме Резерфорда .
Резерфорд выяснил, что центр атома имеет положительно заряженное ядро с диаметром . Оно занимает полного объема атома, но содержит весь положительный заряд и около его массы. Вещество, входящее в состав атома, предполагало наличие плотности , а заряд ядра равнялся суммарному заряду электронов. Было установлено, что при взятии за значение заряда электрона, заряд ядра равнялся числу из таблицы Менделеева.
Планетарная модель
Опыты Резерфорда приводили к радикальным выводам и сомнениям ученых. Используя классическое представление о движении микрочастиц, он предлагает планетарную модель атома. Ее смысл заключался в том, что центр атома состоит из положительно заряженного ядра, которое является основной частью массы элементарной частицы. Атом считается нейтральным. При наличии кулоновских сил вокруг ядра по орбиталям вращаются электроны, как показано на рисунке Электроны всегда находятся в состоянии движения.
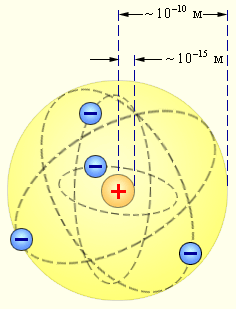
Рисунок Планетарная модель атома Резерфорда. Показаны круговые орбиты четырех электронов.
Предложенная Резерфордом планетарная модель была толчком в развитии знаний о строении атома. Благодаря ей, опыты по рассеиванию -частиц смогли объяснить. Но вопрос об его устойчивости остался открытым. Исходя из закона классической электродинамики, заряд, движущийся с ускорением, излучает электромагнитные волны, забирающие и распределяющие энергию. За время все электроны потратить всю энергию, вследствие чего упасть на ядро. Так как это не происходит, есть объяснение – внутренние процессы не выполняются согласно классическим законам.
Навигация по статьям
