
Статью подготовили специалисты образовательного сервиса Zaochnik.
Квантовые постулаты Бора
Содержание:
В свое время планетарная модель атома была предложена Резерфордом. Фактически, это была неудачная попытка перенести классические представления о движении тел в область явлений атомных масштабов. Планетарная модель оказалась несостоятельной, так как атом неустойчив по причине ускорения, с которым электроны якобы движутся по орбите. В таких условиях электроны должны достаточно быстро растрачивать свою энергию на электромагнитное излучение и падать на ядро.
Рисунок Неустойчивость классического атома.
На смену планетарной теории пришли постулаты Бора. В году выдающийся датский физик Нильс Бор на основе своих наблюдений и фактов, полученных опытным путем, установил, что большая часть представлений о строении атома не соответствовала действительности. Он же стал основоположником новой теории о строении атома.
Рассмотрим два постулата Бора подробнее.
Первый постулат Бора
постулат Бора, который также носит название постулата стационарных состояний, гласит: каждому из стационарных (квантовых) состояний, в котором находится атомная система, соответствует определенный уровень энергии . Находясь в стационарном состоянии, атом не излучает.
В соответствии с классической механикой энергия электрона, движущегося по орбите вокруг ядра, может быть любой. В этом плане первый постулат Бора находится в явном противоречии и с планетарной моделью атома, и с классической механикой.
Постулат стационарных состояний также противоречит и принципам электродинамики, так как допускает возможность ускоренного движения электронов без излучения электромагнитных волн. Все это возможно благодаря системе энергетических уровней. Каждый из уровней соответствует определенному квантовому состоянию. Электрон, который вращается вокруг ядра атома, обладает некоторой механической энергией. В стабильном состоянии атома механическая энергия электрона, который движется по замкнутой траектории вокруг ядра, отрицательная: . Если , то происходит ионизация, т.е. электрон начинает удаляться от ядра.
Состояние с энергией – это основное состояние атома. Величина - это энергия ионизации.
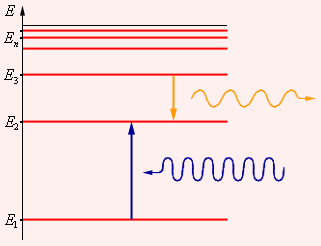
Рисунок Энергетические уровни атома и условное изображение процессов поглощения и испускания фотонов.
Второй постулат Бора
постулат Бора также носит название правила частот. Он гласит, что переход атома из одного квантового состояния, характеризующегося энергией в новое квантовое состояние, которое характеризуется энергией , происходит излучение или поглощение кванта энергии.
Энергия кванта при этом определяется как разность энергий двух квантовых состояний:
,
где – постоянная Планка.
Отсюда можно выразить частоту излучения: .
Правило частот вступает в противоречие с электродинамикой Максвелла, так как частота излучения не зависит от характера движения электрона и определяется только изменением энергии атома. При всех отмеченных нами противоречиях теория Бора не отвергает законов классической физики полностью. В ней по-прежнему используются представления о кулоновском поле ядра и движении электронов по орбитам. Фактически, ядерная модель атома, предложенная Резерфордом, была дополнена Нильсом Бором идеей о квантовании электронных орбит. В связи с этим теорию Бора в некоторых источниках называют полуклассической.
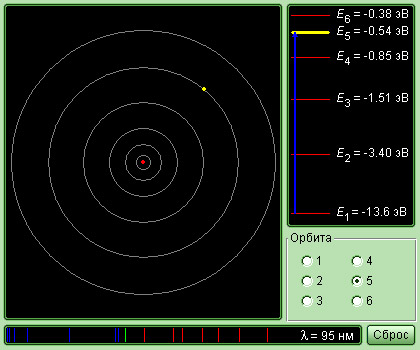
Рисунок Модель постулаты Бора.
Навигация по статьям
